说起抗生素,大家第一个想起的可能就是青霉素,弗莱明发现青霉素的故事很多人也耳熟能详,他也因此获得了1945年的诺贝尔生理学或医学奖。
青霉素杀菌靠的是破坏细菌的细胞壁,让细菌吸水把自己由内而外地炸死。
而最近,来自加拿大麦克马斯特大学的Elizabeth J。 Culp和Gerard D。 Wright等科学家,发现了一种与青霉素作用机制完全相反的两种抗生素——complestatin和corbomycin。它非但不会破坏细菌的细胞壁,反倒让细胞壁变得稳固无比,把细菌活活困死在其中。用个成语来说的话,就是让细菌作茧自缚。
这一研究发表在Nature上[1]。

(来自pixabay.com)
青霉素,被誉为20世纪最伟大的发明之一,在二战那个年代可以说是独一无二的神药,挽救了无数伤兵的性命,甚至一度价比黄金。
后来嘛,抗生素的种类多了,价格也下来了,于是要做手术来一个,咽喉肿痛来一个,感冒发烧来一个,养鸡养鸭来一个。然后,细菌们就耐药了。
耐药了就研发新药吧,然后接着广泛使用,接着产生耐药性,接着研发新药。不过这样的循环估计很快就会被打破了,毕竟1990年后人类就几乎没有发现新的抗生素种类[2],世卫组织也在2017年9月确认世界抗生素濒临枯竭[3]。

二战时的宣传画(来自wikipedia.org)
好在现在生物信息学发达,从基因上筛选新的抗生素成为了可能。研究人员就根据生物合成基因簇和抗生素抗性基因这两方面,试着对糖肽类抗生素展开了筛选。
用来筛选的这两类基因中,生物合成基因好理解,它是微生物用来合成抗生素的。至于抗生素抗性基因,微生物总不能让自己产生的抗生素把自己弄死吧。而糖肽类抗生素的抗性基因,通过靶向修饰起作用,十分独特,易于识别。
通过对基因信息的一步步分析,研究人员确定了两种可能的新抗生素。其中之一是一个已知的化合物complestatin,而另一种则来自采于加拿大亚伯达省的一株链霉菌,被命名为corbomycin。

complestatin和corbomycin的分子结构
这两种新的抗生素的抑菌能力都与糖肽类抗生素的代表——万古霉素——相当,常见的一些耐药菌,比如耐甲氧西林金葡菌,也能杀灭。甚至说对于突破了人类最后一道防线的耐万古霉素肠球菌,complestatin和corbomycin也有活性。
接下来就该搞清楚它俩的杀菌机制了。通常来说,万古霉素等糖肽类抗生素,会作用在细菌细胞壁中的肽聚糖上,阻止细菌细胞壁合成,跟青霉素的作用机制有些类似。不过研究显示complestatin和corbomycin并不能与肽聚糖上的相应位点结合,它们的作用机制与一般的糖肽类抗生素存在差异。
通过进一步的分析和试验,研究人员认为complestatin和corbomycin还是作用在肽聚糖的代谢上,但并没有抑制细胞壁的合成。
不过研究人员发现,在complestatin和corbomycin的最低抑制浓度以下,它们会让细菌的分裂出现异常。细菌细胞本身(原生质体)已经分成了两个,但却没能完成分裂,而是形成一条扭曲打结的细胞链,已知的抗生素中都没发现过这样的现象。
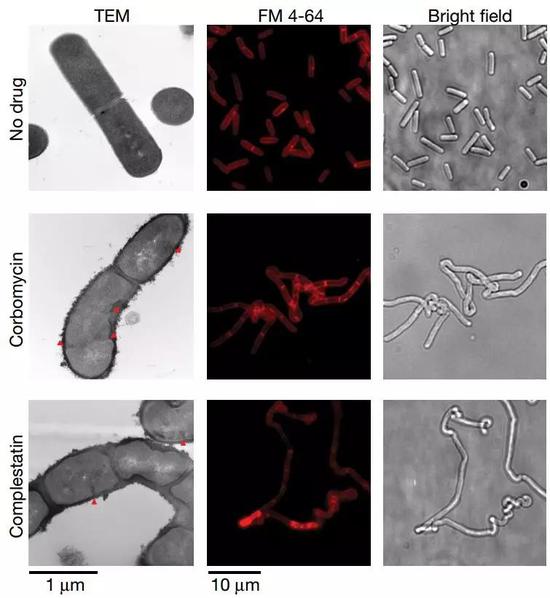
complestatin和corbomycin让细菌长成扭曲打结的一长串
这两个抗生素到底是怎么让细菌长的如此畸形?研究人员尝试通过筛选抗性菌株的方法来找出它们的作用机制。但这一过程却出乎意料的难,金葡菌干脆没有进化出对这两个抗生素的抗性,而枯草杆菌在最低抑制浓度下连续培养了25天,才演化出对这两种抗生素的微弱抗性,让最低抑菌浓度升高了3倍。
通过对产生了抗性的菌株的分析,研究人员认为,这两种抗生素可能阻断了细菌自溶素的功能。
这个自溶素是细菌用来拆开自己的细胞壁的。虽说细胞壁就像细菌的螃蟹壳一样保护了细菌,但细菌还是要长大,还是要分裂,这时候就需要把细胞壁拆开个口子了,如同螃蟹蜕壳一样。而青霉素的杀菌作用,除了抑制细胞壁合成,也恰恰利用了自溶素去拆除现有的细胞壁,让细菌爆炸。
而complestatin和corbomycin,正好可以拮抗青霉素的作用,阻止青霉素作用下细菌的爆炸。在抑菌时,它们也正是抑制了细菌的自溶素,让细菌困死在自己的细胞壁里,展示了一下什么叫做作茧自缚。
这可真是机关算尽太聪明,反误了卿卿性命。你细菌用细胞壁保护自己,我就让你困死在自己的盔甲里。
 站长资讯网
站长资讯网